(Originalartikel unter https://www.astrochymist.org)
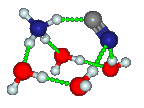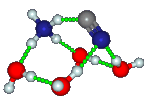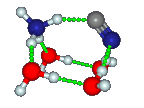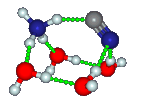
Ammoniumcyanid, NH4CN, wurde, wie 2020 berichtet, von Altwegg und Mitarbeitern in der Koma des Kometen 67P/Churyumov-Gerasimenko nachgewiesen. Dies war eine logische Folge des Nachweises des Ammoniumkations (NH4+) in demselben Kometen im Jahr 2016. Die Identifizierung erfolgte mittels Massenspektroskopie mit dem Rosetta-Spektrometer für Ionen- und Neutralanalyse (ROSINA) auf der Rosetta-Sonde, indem Korrelationen von NH4+ mit anderen Spezies verfolgt wurden.
Eine Reihe weiterer Ammoniumsalze werden auf dem Kometen 67P vermutet: Das Vorhandensein von Ammonium-cyanat (NH4OCN), -chlorid (NH4Cl), -formiat (NH4HCOO) und -acetat (NH4CH3COO) wurde ebenfalls von Altwegg et al. festgestellt, während Ammoniumhydrogensulfid (NH4SH) und -fluorid (NH4F) in einer späteren Veröffentlichung im Jahr 2022 gemeldet wurden. Es gibt auch Hinweise, daß Ammoniumcarbonat oder Ammoniumchloridsalz auf dem Zwergplaneten Ceres vorhanden ist.
Ammoniumcyanid ist ein instabiles Salz. Salze sind ionische Feststoffe, die aus einer Mischung von Kationen und Anionen bestehen, die durch Coulomb-Kräfte aneinander gebunden sind. Es gibt mindestens zwei Möglichkeiten, Paare von neutralen Atomen oder Molekülen in Ionenpaare umzuwandeln: durch Elektronenübertragung und Protonen-übertragung. Bei Salzen, die aus Alkalimetallen und Halogenen gebildet werden, wird ein Elektron vom Metall auf das Halogen übertragen. Dies geschieht selbst dann, wenn sich das einfachste Salzmonomer bildet, wie z. B. das bekannte zweiatomige Astromolekül KCl. Ammoniumcyanid ist ein Beispiel für ein Salz durch Protonentransfer, bei dem Ammoniak H+ aus HCN entfernt und NH4+ bildet, wobei CN– übrig bleibt. Im Gegensatz zu KCl entsteht beim Zusammen-treffen von einzelnen NH3– und HCN-Molekülen in der Gasphase kein NH4CN (NH4+)(CN–). Es ist plausibel, daß sich interstellare und kometare Salze auf Eisoberflächen bilden, wo Wasser die Stabilität der Ionen gegenüber den neutralen Teilchen erhöht. Wie aus der Struktur hervorgeht, ist das einfache NH4CN-Monomer in einem kleinen Cluster selbst bei Anwesenheit einer geringen Menge Wasser rechnerisch stabil.
